Введение
Хирургическое лечение врожденных пороков сердца с функционально единственным желудочком изменилось с момента широкого внедрения операций кавапульмонарного шунта, смысл которых заключается в обходе недоразвитого желудочка и направлении крови полых вен прямо в легочную циркуляцию. Операции двунаправленного анастомоза Гленна (модификация J. Haller), так называемая операция геми-Фонтена (разработанная Marshall Jacobs — выдающимся кардиохирургом, оперирующим сегодня одножелудочковое сердце с нулевой госпитальной летальностью) предполагают выполнение верхнекавапульмонарного анастомоза, а современные модификации оригинальной операции Фонтена, которые выполняются после названных операций, создают перенаправление крови нижней полой вены в легочные артерии либо посредством внутрипредсердного тоннеля (модификация M. R. de Leval), либо с помощью кондуита (метод R. A. Humes и C. R. Marcelletti) (рис. 1-3).
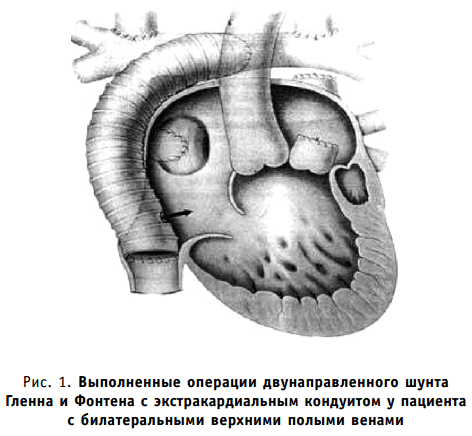
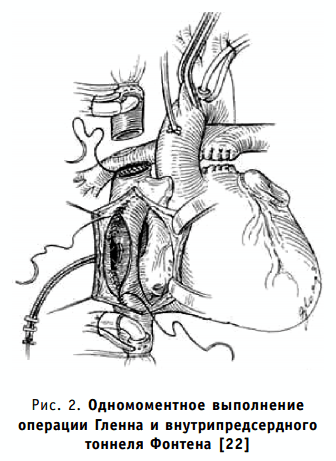
Рис. 3. Выполнение операции геми-Фонтена
В настоящее время исследуются результаты выполнения операции шунта между нижней полой веной и легочной циркуляцией без кондуита по методу Hvass, McKay, Dearani. Общей гемодинамической чертой операций венозно-легочного анастомоза является так называемый парадокс Фонтена: венозная гипертензия и легочная гипотензия. Сегодня изучаются нарушения функции эндотелия у пациентов после операций кава-пульмонарных анастомозов, функции легких, неврологические исходы и качество жизни пациентов.
Нарушения функции печени, поджелудочной железы и почек после операции Фонтена являются наименее изученными осложнениями за 40 лет исследования пациентов с единственным желудочком. По данным системы MEDLINE, имеется всего несколько публикаций по этим темам, причем только одна посвящена нефропатиям у пациентов, перенесших операцию Фонтена.
Этиология и патогенез дисфункции органов пищеварения и мочевыделения и взаимосвязь осложнений
У пациентов с циркуляцией Фонтена центральные венозные давления повышены по причине отсутствия подлегочного насоса, что разделяет системную и легочную циркуляции на отдельные круги. Печень, вклиненная между повышенным давлением центральной венозной системы и портальной венозной циркуляцией, составляет дополнительное капиллярное русло, помимо легочного и интестинального артериального русла. Сердечный выброс также значительно снижен, представляя таким образом идеальный субстрат для развития гепатоцитарной гипоксии, конгестии и стимуляции фибротического ответа. К тому же во время сокращения предсердий наблюдается значительный реверс кровотока с глубоким внутрипеченочным рефлюксом, который ассоциируется с растяжением печеночных вен, вызывая растяжение стромы и сдавление прилежащих пластов гепатоцитов. Механодеструкция, ассоциированная с растяжением и компрессией, может быть потенциальным индуктором и/или модулятором фиброза печени.
KauLitz, Bergman, Lihmer (1999) зафиксировали влияние повышенного предсердного и системного давлений на функцию печени и почек. У пациентов после операции Фонтена и у других больных с высокими венозными давлениями выявлены патологические нарушения ферментов печени.
Помимо самой циркуляции Фонтена, на функцию органов пищеварения и мочевыделения и на морфологические изменения в тканях оказывают влияние перенесенная пациентом глубокая гипотермическая остановка циркуляции и кардиопульмонарный байпасс, а также интоксикация медикаментами: анестетиками, антиаритмиками, варфарином, аспирином (как известно, с ним у детей ассоциируется синдром Рейе). Считается, что больные с кавапульмонарной циркуляцией особенно предрасположены к панкреатиту с показателем смертности в 50% — патологии, которая нередко развивается у взрослых пациентов после операций с применением кардиопульмонарного байпасса (КПБ).
Syed et al. (2005) пришли к заключению, что нарушенная вентрикулярная релаксация и сниженный сердечный выброс до операции предсказывают повышенный риск развития панкреатита у пациентов с циркуляцией Фонтена. Ben-Shachar et al. (1981) сообщили о развитии панкреатита у пациента с обструкцией кондуита, что привело к смерти. Tomita et al. (2004) сообщили о случае развития респираторного дистресса, острой почечной недостаточности и геморрагического панкреатита у пациента со сдавлением кондуита медиастинальной гематомой, который также завершился смертельным исходом.
Premchand et al. (2008) исследовали группу из 21 пациента, перенесших операцию Фонтена 11,4 ± 6,5 года назад с историей нормального УЗИ и сопутствующих заболеваний, которые могли бы повлиять на функцию почек. Список медикаментов, которые получали пациенты, включал аспирин (14 пациентов), коумадин (8 чел.), эналаприл (8 чел.), лизиноприл (10 чел.), дигоксин (11 чел.), диуретики (5 чел.), бета-блокаторы (5 чел.); 4 пациента имели водитель ритма. У всех отмечались нормальное давление и уровень клубочковой фильтрации. У 9 пациентов (43%) наблюдалось патологическое соотношение микроальбумина и креатинина (больше 20 мкг/мг). Основной находкой исследования явился тот факт, что у пациентов, которые принимали лизиноприл-эквивалентную дозу ингибитора АПФ в количестве более 0,4 мг/кг/сут., не наблюдалось патологической микроальбуминурии, что свидетельствует о нефропротекторном эффекте этой группы препаратов. Интересно отметить, что в одном исследовании ингибиторы АПФ не показали свою эффективность как средства, улучшающего переносимость физической нагрузки у пациентов с циркуляцией Фонтена.
Микроальбуминурия является самым ранним индикатором гломерулопатии и рутинно применяется для мониторинга начала и прогрессирования болезней почек. У пациентов с диабетом присутствие микроальбуминурии связывается с увеличением сердечно-сосудистой смертности и заболеваемости от 2 до 4 раз. Данные исследования позволяют считать, что повреждение почек связывается с повышенным центральным венозным давлением, которое известно как фактор, повышающий эфферентное артериальное давление и снижающий афферентный артериальный кровоток, что повышает фильтрационное давление внутри клубочка и приводит к микроальбуминурии. Этот феномен показан в эксперименте Doty et al. Другими причинами потери белка могут быть низкий сердечный выброс и повреждение почек кардиопульмонарным байпассом и нефротоксическими медикаментами. Однако в указанном исследовании наблюдалась нормальная вентрикулярная функция, а острое повреждение почек имело место только у одного пациента. Эти факты снижают вероятность значимости других причин, кроме высокого центрального давления, в патогенезе микроальбуминурии.
Патологическая анатомия повреждения печени
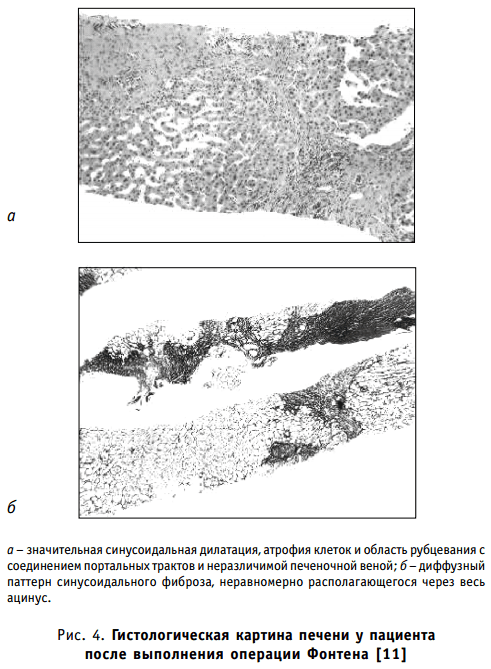
Повреждение печени, которое может быть распространенным у пациентов этой группы, связано с продолжительностью функционирования циркуляции Фонтена и давлением печеночных вен. Печеночный фиброз и цирроз с риском развития желудочно-пищеводных варикозных и регенеративных печеночных узлов, предшественник гепатоцеллюлярной карциномы, это обычная находка у таких пациентов (рис. 4).
Диагностические данные
Chaloupecky et al. (2005) отметили, что почти у половины пациентов после выполнения тотального кавапульмонарного анастомоза имелись лабораторные признаки умеренного холестаза. Наблюдался сниженный синтез печенью прокоагулянтных факторов, однако у отдельных пациентов с хорошим исходом выявлялся сбалансированный общий коагуляционный гомеостаз.
По данным Narkewicz et al. (2003), аномальная функция печени, преимущественно отображающая холестаз, выявлялась у 21 пациента, которые находились под наблюдением сравнительно длительный период времени (р < 0,01). Синтез протеинов оказался нормальным почти у всех пациентов. Коагуляционный профиль показал аномалии у 22 пациентов. «Прокоагулянтные» аномалии, такие как сниженный плазминоген и активный протеин С, отмечались у 11 и 5 пациентов соответственно. Масштаб этих нарушений (абнормалий) у пациентов уменьшился в более отдаленные сроки наблюдения. Антикоагулянтные аномалии, такие как недостаточность пятого и седьмого факторов, выявлены у 16 и 17 пациентов соответственно, что привело к пролонгированному протромбиновому времени у 19 пациентов. 13 пациентов имели как про-, так и антикоагулянтные аномалии.
Протромботическое состояние отмечалось у 5 пациентов со сравнительно более длительным интервалом времени с момента операции (р = 0,05). Таким образом, хотя индивидуальные прокоагулянтные показатели снижаются по мере увеличения срока с момента выполнения операции, протромботическое состояние выявляется именно у пациентов в наиболее отдаленные сроки наблюдения. Авторы пришли к выводу, что умеренный холестаз присутствовал преимущественно у пациентов с циркуляцией Фонтена, которые подвергались длительному наблюдению. Наряду с лабораторными прокоагулянтными аномалиями, показывающими протромботическое состояние, диагностировались и антикоагулянтные нарушения. Коагуляционный профиль варьировался в различные интервалы времени после операции. Согласно наблюдениям, наиболее распространенным биохимическим нарушением функции печени являются удлинение протромбинового времени и низкий уровень пятого фактора. Имелась тенденция к прогрессирующему нарушению показателей протромбинового времени по мере увеличения интервала с момента выполнения операции Фонтена.
Однако при длительном наблюдении у большинства обследуемых пациентов отмечались нормальные или немного повышенные уровни аминотрансферазы плазмы. Уровни гамма-глютамилтранспептидазы часто немного повышены, в то время как уровень билирубина оказался нормальным у всех обследуемых пациентов. В исследовании Сheung et al. (2006) 29% пациентов имели уровни билирубина крови, превышающие верхнюю границу нормы. С другой стороны, отмечались нормальные значения альбумина плазмы, аспартат аминотрансферазы, аланин аминотрансферазы и щелочной фофатазы.
Лечение и профилактика
Потенциально сосудорасширяющая терапия может уменьшить транспеченочный и транслегочной градиент. Недавно установлено, что силденафил (ингибитор фосфодиестеразы 5 типа) и бозентан, неселективный блокатор рецепторов эндотелия, показали свою эффективность, благоприятно модулируя легочное сосудистое сопротивление. В контексте циркуляции Фонтена они могут улучшить чрезпеченочные перфузионные давления. Неизвестно, оказывают ли эти препараты влияние на сопротивление сосудов печени, но исследователи считают, что состояние пациентов с болезнью печени наверняка улучшится после выполнения фенестрации. Однако эта идея требует проспективной оценки, прежде чем могут быть сделаны общие рекомендации.
Нам не удалось найти сообщений об опыте применения стандартных медикаментов для лечения нарушения функции печени у пациентов с единственным желудочком — таких, например, как эссенциальные фосфолипиды, адметионин, липоевая кислота, экстракты расторопши, урсодезоксихолиевая кислота, адсорбенты, лактулоза, витамины и минеральные воды, пирацетам и пентоксифиллин (для улучшения кровообращения и детоксикации). Можно предположить, что применение указанных препаратов окажет положительное влияние на самочувствие пациентов, на их рост, развитие, неврологический статус, а также на снижение смертельных тромбоэмболий и, что самое главное, улучшит качество жизни выздоравливающего.
Заключение
Основной закономерностью кавапульмонарной циркуляции с повышенным венозным давлением и низким сердечным выбросом является потеря протеинов крови как через дыхательные пути, вены и лимфатический проток (при пластическом бронхите и плевральной транссудации) и кишечник (протеинтеряющей энтеропатии), так и через почки, как показывает пока единственное исследование. Очевидно, что этот феномен негативно влияет на результаты операций. У таких пациентов необходимы методы профилактики и лечения нарушений функций внутренних органов. Учитывая схожий патогенез названных осложнений, можно рассчитывать, что средства и методы, эффективные при одном из них, помогут при другом. Например, силденафил, кальций, октреотид, глюкокортикоиды, сравнительно эффективные для протеинтеряющей энтеропатии, возможно, могут уменьшить и потерю белка через почки. Вероятно, что улучшение функции одного органа улучшит функцию другого, что в итоге приведет к улучшению состояния пациентов и продлит их жизнь.
Спринджук М. В. РНПЦ «Кардиология», г. Минск.
Опубликовано: «Медицинская панорама» № 5, апрель 2008.