Cахарный диабет (СД), особенно 2 типа, является проблемой медицины, актуальность которой неуклонно возрастает. Это обусловлено прогрессивным увеличением количества больных, существенно превышающим прогнозные показатели, и увеличением продолжительности жизни с диабетом. XXI век является таким периодом в развитии медицины, который характеризуется направленностью на оптимизацию качества жизни, а не только на ликвидацию симптомов болезни и увеличение продолжительности жизни. С этих позиций особое значение приобретает состояние половой функции как у женщин, так и у мужчин.
По данным ВОЗ, в 2002 г. средняя продолжительность жизни мужчин оказалась выше, чем у женщин, только в 6 странах мира: Непале, Ботсване, Зимбабве, Лесото, Бангладеш и Свазиленде. В 2005 г. проф. Дэнни Дорлинг (Великобритания) установил, что в мире больше не осталось стран, где мужчины жили бы дольше женщин.
Что связывает СД 2 типа и половую функцию?
В настоящее время доказано, что возрастной андрогенный дефицит (Late Onset Hypogonadism) является характерным проявлением состояния зрелого мужчины. Во многих исследованиях (Массачусетское, HIM и др.) доказывается, что в возрасте старше 45 лет регистрируется прогрессивное снижение андрогенной функции, сопровождающееся снижением уровня общего и свободного тестостерона, возрастанием уровня секссвязывающего глобулина. При этом отмечается, что риск снижения уровня тестостерона выше в 2,7 раза при индексе массы тела > 27 кг/м2, в 2,1 раза — при СД, в 1,8 раза — при наличии артериальной гипертензии.
Известно, что СД 2 типа, характеризующийся инсулинорезистетностью (ИР), в большинстве случаев манифестирует в возрасте старше 40 лет, что исходно подразумевает его одновременное развитие с возрастным андрогенным дефицитом. Метаболическая связь этих двух состояний может быть объяснена вовлечением в патологический процесс висцеральной жировой ткани, которая является эндокринным органом, участвующим в продукции острофазных белков — маркеров воспаления (CRP, PAI-1, сывороточного амилоида А), маркеров воспаления (TNF-a, IL-1, IL-6, IL-8, IL-10), гормонально-активных веществ, оказывающих влияние на энергетический баланс организма (адипонектин, лептин, резистин, висфатин), тканевых факторов, ассоциированных с активностью фибринолиза, регуляцией сосудистого тонуса (ангиотензиноген, VEGF), факторов, влияющих на липидный профиль крови (АроЕ, свободные жирные кислоты, липопротеиды). Кроме того, в висцеральной жировой ткани происходит конверсия кортизона в кортизол и андрогенов в эстрогены. Не требуется дополнительных доказательств в том, что именно висцеральная жировая ткань является причиной инсулинорезистетности, поскольку этот факт уже является аксиомой.
Поскольку висцеральная жировая ткань в то же время является местом конверсии андрогенов в эстрогены, несомненный интерес представляет вероятность ассоциации ожирения и возрастного андрогенного дефицита. Рабочая гипотеза о том, что низкий уровень тестостерона ассоциирован с риском развития метаболического синдрома и может инициировать манифестацию СД 2 типа и сердечно-сосудистую патологию, высказана Laaksonen DE (Diabetes Care, 2004, 27: 1036-1041) на основании существующих исследований, подтверждающих, что тестостерон и дигидротестостерон ингибируют превращение полипотентных стволовых клеток в адипоциты (Singh, 2003).
Проведенные клинические исследования подтвердили правомочность этой гипотезы: частота СД 2 типа выше у мужчин с низким уровнем тестостерона, низкий уровень тестостерона ассоциирован с высоким риском метаболического синдрома и ожирения, в то время как высокий уровень тестостерона связан с высоким уровнем чувствительности к инсулину и снижением риска СД 2 типа. Как показано в исследовании PROCAM, у пациентов, имеющих СД, уровень общей смертности, смертности от ИБС, частота ИБС и мозгового инсульта значительно выше, чем у лиц без метаболических нарушений. В рамках Фрамингемского исследования впервые показано, что ожирение и метаболический синдром значимо и независимо увеличивают частоту ССЗ и сердечно-сосудистых осложнений прежде всего у мужчин с избыточным весом (ИМТ от 25,0 до 29,9 кг/м2), у которых артериальная гипертензия (АГ) выявлялась на 75%, а у женщин — только на 46% чаще по сравнению с лицами без избыточного веса.
До настоящего времени не существует единого мнения по поводу первопричины метаболических нарушений в патогенезе метаболического синдрома. Одни авторы считают, что наследственная предрасположенность к инсулинорезистентности и ожирению в сочетании с низкой физической активностью и избыточным питанием определяют развитие ожирения и тканевой инсулинорезистентности и, как следствие — компенсаторной гиперинсулинемии. Гиперинсулинемия сначала снижает чувствительность, а затем блокирует инсулиновые рецепторы, вследствие чего поступающие с пищей глюкоза и жиры депонируются в жировой ткани. Это еще больше усиливает инсулинорезистентность. С другой стороны, гиперинсулинемия подавляет распад жиров, что способствует прогрессированию ожирения. Образуется порочный круг. Постоянная гиперинсулинемия истощает секреторный аппарат β-клеток поджелудочной железы, что приводит к нарушению толерантности к глюкозе.
Однако существует и другая гипотеза, в соответствии с которой предполагается, что причиной инсулинорезистентности, гиперинсулинемии и других метаболических нарушений выступает центральный тип ожирения. Адипоциты висцеральной жировой ткани секретируют свободные жирные кислоты непосредственно в воротную вену печени. Их высокие концентрации подавляют поглощение инсулина печенью, что приводит к гиперинсулинемии и относительной инсулинорезистентности.
Повышение артериального давления (АД) обнаруживается у 80% больных с СД 2 типа. В последнее время обсуждается еще одна теория патогенеза АГ при ожирении, согласно которой рост АД обусловлен повышением уровня лептина у таких больных. Лептин является гормоном, синтезируемым адипоцитами висцеральной жировой ткани, и его уровень тесно коррелирует с индексом массы тела (ИМТ). Лептин регулирует чувство насыщения на уровне дугообразного ядра гипоталамуса, тесно связанного с паравентрикулярным ядром, стимуляция которого приводит к активации симпатической нервной системы.
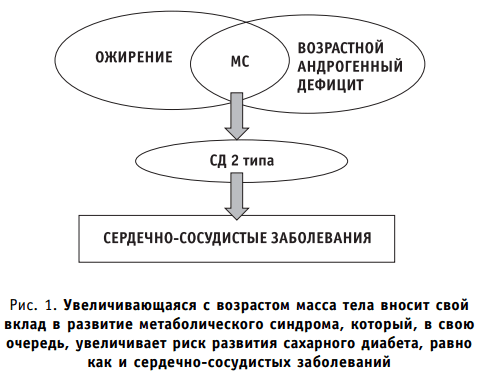
Таким образом, суммируя приведенные факты, следует полагать, что низкая концентрация свободного тестостерона, приводя к повышению маркеров воспаления, способствует развитию и прогрессированию ожирения и атеросклероза, многократно повышая кардиоваскулярный риск у мужчин. Исходя из этого, можно предположить, что нормализация уровня тестостерона способствует регрессу метаболических нарушений не только за счет усиления липолиза, повышения физической активности, повышения чувствительности тканей к инсулину, но также и посредством подавления воспалительного ответа.
Материал и методы
На базе ГУ «РНПЦ радиационной медицины и экологии человека» (РНПЦ РМ и ЭЧ) начато исследование по проблеме возрастного андрогенного дефицита. К участию в проекте приглашены мужчины с СД 2 типа в возрасте от 45 до 60 лет. Из исследования исключались: пациенты с раком предстательной железы, раком молочной железы, сердечной недостаточностью (Н II Б и более), острой коронарной патологией, острым нарушением мозгового кровообращения, гинекомастией, хронической обструктивной болезнью легких, заболеваниями щитовидной железы, почечной недостаточностью, печеночной недостаточностью, ВИЧ.
Перед включением в исследование у всех пациентов проводилось анкетирование и осмотр с антропометрическими измерениями (рост, вес, ИМТ, общий тестостерон, ОБ, Т/Б); для верификации осложнений — ретинопатии, нейропатии, нефропатии, сердечно-сосудистых заболеваний — исследовались уровни общего тестостерона (ОТ), SHBG (глобулин, связывающий половые стероиды), свободного тестостерона (свТ), ЛГ, ФСГ. Определение концентрации половых гормонов (эстрадиола, прогестерона, тестостерона, пролактина, лютеотропного и фолликулостимулирующего) осуществлялось с помощью автоматического гамма-счетчика «1470 WIZARDTM» (Wallac, Финляндия). Уровень свободного и биодоступного тестостерона (bT) определялся расчетным методом с помощью общего тестостерона и SHBG по методу Vermeulen et al. с использованием специальной компьютерной программы и веб-сайта (solvay-pharma.ru).
Статистическая обработка материала, построение графиков и таблиц производились с использованием StatSoft Statistica 7,0 (Windows). Статистическую значимость результатов исследования оценивали методами параметрической и непараметрической статистики. Тест Mann Whitney использовался для сравнения непараметрических данных и проверки гипотезы о различии в независимых выборках. Fisher exact test, или χ2-test, использовался также для сравнения соответствующих групп при анализе таблиц сопряженности. Для выявления корреляций использовалась корреляция Спирмена (для непараметрических данных). Множественный регрессионный анализ применялся в том случае, если в наличии оказывался один независимый признак. Достоверными считались различия при р
Для оценки уровня андрогенной обеспеченности нами обследовано 50 пациентов с СД 2 типа в возрасте от 45 до 60 лет (средний возраст составил 53,57 ± 4,95 года). Стаж диабета — 8,53 ± 5,33 года (от 1 мес. до 20 лет), ИМТ — 31,6 ± 4,9 кг/м2, HbA1C — 8,5 ± 1,8% (7-12,4%). Группа контроля включала 25 здоровых человек из той же возрастной категории.
Результаты и обсуждение
По результатам данных опросника для оценки андрогенного статуса мужчины, распространенность гипогонадизма составила 100%, что может объясняться относительно небольшой выборкой. При этом невыраженные симптомы андрогенного дефицита обнаруживались у 2%, слабо выраженные — у 28,5, средней выраженности — 36,7 и выраженные — у 32,7% обследуемых. В контрольной группе 10% опрошенных имели невыраженные, 30,5 — слабо выраженные, 34,7 — средней выраженности и 24,8% — выраженные симптомы андрогенного дефицита.
Уровни общего тестостерона и SHBG составили соответственно 11,9 ± 7,2 и 39,2 ± 15,3 нмоль/л. При этом у 63% (n = 31) обследованных уровень общего тестостерона определялся 0,3).
При проведении статистического анализа достоверных корреляций между баллами опросника и уровнем общего тестостерона или свободного тестостерона не выявлено, но при сравнении уровней общего тестостерона и свободного тестостерона в группах больных с гипогонадизмом и без такового выявлены достоверные различия для общего тестостерона (р = 0,00001). Уровень свободного тестостерона составил 1,9 ± 0,45 нмоль/л (нормальные значения 1,08-3,16 нмоль/л), уровень биодоступного тестостерона — 45,07 ± 10,6 нмоль/л (нормальные значения 25,3-74 нмоль/л).
Обследованные мужчины были разделены на 3 возрастные группы:
- 1 группа — 45-49 лет,
- 2 группа — 50-55 лет,
- 3 группа — 56-60 лет.
Уровни общего тестостерона, биодоступного тестостерона и SHBG в различных возрастных группах представлены на рис. 2.
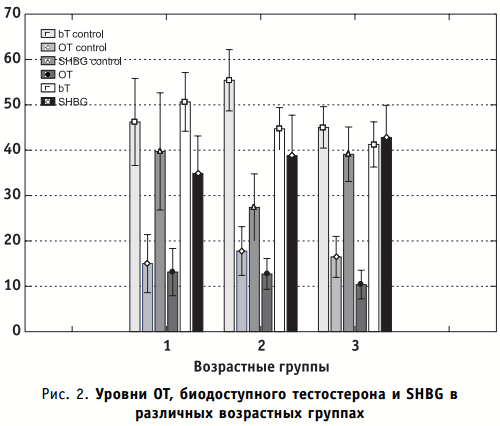
Снижение bT, по сравнению с общим тестостероном, оказалось достоверным в 1 и 3 возрастных группах (р
Уровни ЛГ, ФСГ, пролактина составили соответственно 6,7 ± 5,3, 5,08 ± 3,17, 9,92 ± 4,65 мМЕ/мл. При индивидуальной оценке отмечено, что выше нормы оказался уровень ФСГ у 10 пациентов, уровень ЛГ — у 6 (при этом 3 чел. имели одновременно высокие уровни ЛГ и ФСГ); уровень пролактина у всех пациентов наблюдался в норме. Таким образом, в большинстве случаев у обследуемых больных снижение концентрации тестостерона не сопровождалось повышением уровня гонадотропинов, что свидетельствует о дисфункции системы гипоталамус-гипофиз-яички. Результаты оценки исследуемых параметров от ИМТ приведены в табл. 1.
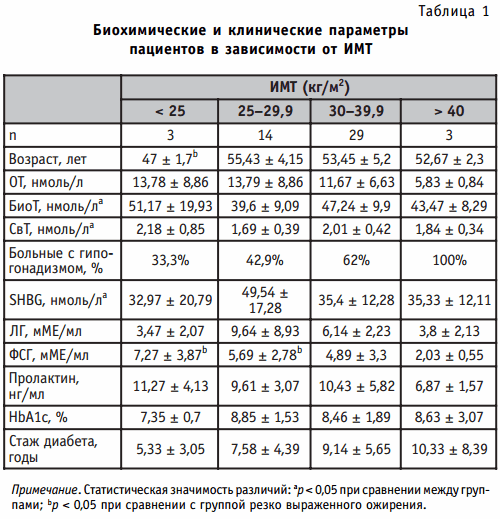
Уровень общего тестостерона отрицательно коррелировал с ИМТ (r = -0,294; р 1C (r = -0,303; р
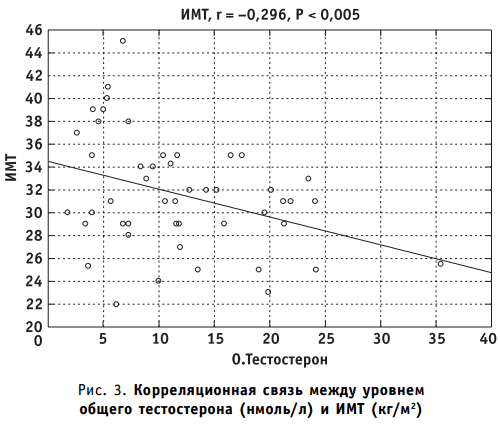
Не выявлено корреляции между уровнями общего тестостерона, ФСГ, пролактина, HbA1C, возрастом в зависимости от метода лечения (инсулинотерапия или таблетированные сахароснижающие препараты).
Таким образом, полученные нами данные свидетельствуют о крайне высокой распространенности возрастного андрогенного дефицита и развитии гипогонадизма у больных СД 2 типа, превышающей 63% и увеличивающейся с возрастом пациента и длительностью заболевания. При этом наличие гипогонадизма у больных СД 2 типа приводит к расстройствам психоэмоционального статуса и половой функции, что снижает качество жизни больных СД и уменьшает психологическую мотивацию к его компенсации. Последнее обстоятельство, в свою очередь, чревато ухудшением углеводного обмена и нарушением метаболизма липидов. В связи с этим необходимо принять меры, направленные на активное выявление гипогонадизма у больных СД 2 типа, и, при наличии показаний, провести патогенетическую заместительную терапию, направленную на его устранение. С учетом высокой распространенности андрогенного дефицита у мужчин с метаболическим синдромом и СД 2 типа, а также негативного влияния дефицита тестостерона на поддержание ожирения и основные компоненты метаболического синдрома (дислипидемия, инсулинорезистентность и артериальная гипертензия), у всех мужчин с данными состояниями должно проводиться гормональное обследование, включающее определение уровней тестостерона, ЛГ и SHBG.
Коррекция тестостероновой недостаточности позитивно сказывается на течении таких заболеваний, как сахарный диабет, ишемическая болезнь сердца, сердечная недостаточность, также она препятствует развитию остеопороза. В настоящее время в мире накоплен определенный опыт по использованию заместительной гормональной терапии андрогенами в лечении возрастного андрогенодефицита. Доказано, что большинство больных с недостатком тестостерона отмечают значительное повышение физической активности, уменьшение депрессии, увеличение полового влечения (либидо), увеличение мышечной массы и силы мускулатуры, уменьшение висцеральных жировых отложений, снижение уровня холестерина в крови.
В то же время не существует единого мнения по поводу того, на каком уровне нужно поддерживать циркулирующий тестостерон в процессе заместительной терапии (с учетом эффективности и безопасности). Также дискутируются возможности использования различных лекарственных форм тестостерона. Большинство клиницистов считают, что целевые уровни тестостерона не должны быть суперфизиологическими при сохранении суточного ритма тестостерона. В настоящее время используются внутримышечные инъекции эфиров тестостерона или ундекоата, таблетки тестостерона ундеканоата, а также трансдермальный тестостерон в виде пластыря или геля. Недостатками инъекционных препаратов тестостерона являются боль и дискомфорт в месте инъекции, а также повышение через 24-48 ч после инъекции уровня тестостерона выше физиологического и снижение его ниже порогового перед следующей инъекцией и возможные гепатотоксические влияния. Значимым недостатком инъекционного лечения является «неуправляемость» введенного внутримышечно тестостерона, особенно у мужчин старше 50 лет, в случае возникновения необходимости срочного прекращения или уменьшения его действия.
Международные эксперты указывают на необходимость использования у пациентов с возрастным гипогонадизмом андрогенных препаратов короткого действия, при отмене которых, в случае возникновения противопоказаний, уровень тестостерона быстро снижается до исходного. Этим требованиям отвечают трансдермальные формы тестостерона, среди которых максимальная комплаентность обеспечивается при использовании гелевых форм. В настоящее время используется тестостерон, содержащий гидроалкогольный гель («Андрогель»), который применяют 1 раз в день путем нанесения на кожу. Важнейшим преимуществом гелевых форм тестостерона является отсутствие супрафизиологических пиков концентрации тестостерона в крови и возможность прекращения лечения по необходимости. Безусловно, лечение препаратами экзогенного тестостерона требует динамического наблюдения и предварительного обследования.
Последние годы ознаменовались повышенным вниманием специалистов к заместительной терапии при мужском возрастном андрогеном дефиците, назначаемой для поддержания андрогензависимых функций. Приведенные нами результаты обследования больных СД 2 типа свидетельствуют, что эта категория больных нуждается в специальном обследовании и, возможно, лечении. Мы планируем провести анализ исследуемых показателей в процессе андрогензаместительной терапии.
Василькова О. Н., Мохорт Т. В., Шаршакова Т. М., Буланов В. И., Романов Г. Н.
Гомельский государственный медицинский университет; Белорусский государственный медицинский университет; ГУ «РНПЦ радиационной медицины и экологии человека».
Опубликовано: «Медицинская панорама» № 5, апрель 2008.