Тремор (дрожание) - непроизвольные насильственные ритмичные колебательные движения части тела вокруг фиксированной точки в пространстве, которые вызываются сокращениями групп мышц-антагонистов. Тремор преобладает в структуре непроизвольных движений человека и по локализации относится к гиперкинезам преимущественно стволового уровня. Тремор является полиэтиологическим синдромом и встречается в клинической практике врачей многих специальностей (неврологов, эндокринологов, психиатров и т.д.). Тремор имеет две основные характеристики: частота колебаний и их амплитуда, определяемая величиной смещения части тела вокруг фиксированной точки.
По частоте колебаний дрожание может быть условно разделено на 3 группы:
- низкочастотное (3-5 Гц),
- среднечастотное (5-8 Гц),
- высокочастотное (9-12 Гц).
По амплитуде дрожание делится на:
- низкоамплитудное,
- среднеамплитудное,
- высокоамплитудное.
Выделяют фокальный либо генерализованный тремор, при котором одновременно поражаются конечности, голова, нижняя челюсть, голосовые связки, язык. Подобные нарушения существенно ухудшают качество жизни и адаптацию этих пациентов в обществе.
В клинической работе невролога практическое значение имеет выделение следующих видов тремора: покоя, постурального и кинетического. Тремор покоя (статический тремор) имеет частоту 3-6 Гц и наиболее характерен для болезни Паркинсона или дегенеративных заболеваний ЦНС. Постуральный (антигравитационный) тремор характеризуется частотой 5-9 Гц, выявляется в положении с вытянутыми вперед руками и имеет место при синдроме отмены алкоголя, некоторых лекарственных препаратов, при обменных нарушениях, а также может быть психогенным или физиологическим. Кинетический тремор имеет частотную характеристику 3-10 Гц, подразделяется на тремор сокращения, проявляющийся при изометрическом напряжении мышц (при сжатии кисти в кулак) и интенционный тремор, возникающий при целенаправленном движении конечности (например, при выполнении пальценосовой пробы). Этот тип характерен для тремора Минора, поражения ствола мозга или мозжечка различного генеза (рассеянный склероз, опухоль, гематома). Вариантом кинетического тремора является task-specific tremor (тремор при выполнении определенного действия), появляющийся при выполнении точных мелких движений, таких как застегивание украшений, работа с маленькими деталями и т.п.
Клинические проявления тремора
Клинические проявления тремора полиморфны и встречаются при широком круге неврологических заболеваний. По этиологическому принципу виды тремора подразделяются на:
Физиологические: нормальный и усиленный тремор.
Патологические виды тремора:
- эссенциальный (наследственный и спорадический);
- паркинсонический;
- дистонический;
- мозжечковый (интенционное дрожание);
- тремор Холмса (среднего мозга или рубральный);
- невропатический;
- психогенный.
Физиологический тремор (асимптомное дрожание) встречается у любого здорового человека при волнении, характеризуется частотой 8-12 Гц в руках и менее чем 6,5 Гц в других частях тела. Усиленный физиологический тремор отличается от физиологического большей амплитудой и чаще встречается при гиперадренергических состояниях (эмоциональный стресс, эндокринные нарушения), во время приема ряда лекарственных препаратов или алкоголя. Особенностью данного вида тремора является его значительное уменьшение или полное исчезновение при назначении β-блокаторов.
Патологический тремор. Наиболее распространенной причиной патологического тремора является эссенциальный тремор Минора, частота и степень выраженности которого увеличивается с возрастом. Этот вид может быть как наследственным (аутосомно-доминантный тип наследования с вариабельной пенетрантностью) и, соответственно, проявляться в нескольких поколениях одной семьи, так и манифестироваться спорадически у членов одной семьи. Частота эссенциального тремора составляет 4-11 Гц и зависит от того, какой сегмент тела поражен. Проксимальные сегменты характеризуются низкими частотами, дистальные - более высокими. Наиболее часто поражается голова и/или кисти рук. Для данного вида тремора характерен постуральный и кинетический компонент. Тремор Минора может представлять самостоятельную нозологическую форму, реже - сопровождать различные нарушения движений, например паркинсонизм или фокальную дистонию.
Паркинсонический тремор возникает в покое, характеризуется частотой 4-6 Гц, средней амплитудой и чаще встречается в пальцах кистей. Реже (в порядке убывания) поражаются нижняя челюсть, губы, язык, ноги, голова, туловище. Изолированный паркинсонический тремор головы не встречается. Тремор кистей при болезни Паркинсона ассиметричен, при письме, как правило, усиливается. При движении тремор прекращается или значительно уменьшается, но после остановки возобновляется. В медицинских публикациях такой тремор часто называют «счетом монет» или «скатыванием пилюль».
Ортостатический тремор является редким расстройством движения. Характеризуется дрожанием ног в положении стоя и исчезает при ходьбе, сидении или в положении лежа. Отличительной особенностью данного вида тремора является его высокая частота: 14-16 Гц. В положении стоя у пациента может определяться подергивание четырехглавой мышцы бедра.
Дистонический тремор представляет собой дрожание части тела, в которой локализован дистонический синдром. Для данного вида тремора характерна нерегулярная амплитуда и вариабельная частота, часто - подверженность модулирующему влиянию позы.
При треморе Холмса (рубральном треморе) представлены все 3 основных типа дрожания, которые отличаются степенью выраженности. Данный тип возникает при повреждениях среднего мозга (инсульт, ЧМТ, опухоль или рассеянный склероз). Его частота составляет 2-5 Гц.
Мозжечковый (интенционный) тремор является кинетическим и проявляется при выполнении произвольного акта. Его развитие связано с нарушением корригирующего влияния мозжечковых систем на двигательный акт вследствие повреждений, локализующихся в латеральных мозжечковых ядрах или в верхней ножке мозжечка, либо в местах их соединений. При поражении срединных структур мозжечка развивается тремор в руках, голове и туловище. При клиническом осмотре выраженность тремора различается от небольших толчкообразных движений, до крупных, переходящих в мозжечковую хорею или асинергию.
Невропатический тремор имеет место при врожденных или приобретенных невропатиях и клинически напоминает эссенциальный тремор. Причиной дрожания является нарушение проприоцептивной чувствительности. Характерной чертой невропатического тремора является его усиление при выполнении задания (пальценосовой пробы и др.) с закрытыми глазами.
Психогенный тремор - наиболее сложный вид дрожания, поскольку требует исключения его органической природы. Данный вид может быть постуральным, а может проявляться в покое или при движении. Клинически психогенный тремор характеризуется внезапным началом, спонтанной ремиссией, стационарным течением и неклассифицируемыми видами тремора.
Диагностика тремора
Диагностика тремора основана на объективных тестах и инструментальных методах исследования. К широко известным объективным тестам относятся: рисование спирали, наливание воды из чаши, шкалы оценки тремора, тест лабиринта Гибсона. Инструментальные методы исследования включают позитронно-эмиссионную томографию, поверхностную электромиографию (ЭМГ), оптические методики и акселерометрию. Позитронно-эмиссионная томография позволяет с помощью меченых изотопов (F18, O15) проследить за изменением уровня регионарного кровотока и оценить локализацию вовлечения нейронов. Поверхностная суммарная ЭМГ регистрирует запись залпов определенной частоты и амплитуды, которые чередуются с участками изолинии. Оптические методики основаны на использовании источника света и регистрирующего устройства.
Современным методом регистрации тремора является акселерометрия. Методика основана на использовании специальных датчиков - акселерометров, измеряющих линейное ускорение, характерное для всех движений (кроме случаев с постоянной скоростью). Получаемые сигналы с помощью аналогово-цифрового устройства преобразуются в цифровые и поступают в компьютер. Специальными программами производится их обработка, что позволяет построить графическую зависимость перемещения датчиков во времени, уточнить частотную и амплитудную характеристику движения.
Лечение тремора
Выделяют этиотропное, патогенетическое и симптоматическое лечение тремора. В современной клинической практике наиболее распространена симптоматическая терапия дрожания, выбор которой зависит от типа тремора.
Препаратами выбора коррекции кинетического тремора являются β-блокаторы, бензодиазепины или вальпроаты. Механизм воздействия β-блокаторов (анаприлин, пропранолол) на дрожание окончательно не изучен. Препарат назначают в начальной дозе 10 мг 3 раза в день, с постепенным повышением до максимальной дозы 240 мг/сут. По данным Koller W. C., пропранолол в дозе 160 мг/сут уменьшает амплитуду тремора на 50-70%. Среди недостатков лечения β-блокаторами - относительно высокая частота отмены лечения (в основном из-за возникновения повышенной утомляемости и брадикардии) и невозможность резкого прекращения их приема. Бензодиазепины (диазепам, клоназепам) воздействуют на тремор за счет своего противосудорожного и миорелаксирующего эффектов. Дозировка подбирается индивидуально и обычно составляет 4-6 мг/сут. Побочными эффектами бензодиазепинов являются головокружение, сонливость, возможное привыкание. Соли вальпроевой кислоты (производные натриевой и кальциевой соли) оказывают влияние на тремор посредством воздействия на обмен гамма-аминомасляной кислоты. Их суточная доза составляет 300-600 мг/сут. Побочные эффекты этих медикаментов - тошнота и диарея.
С целью влияния на тремор покоя применяют антихолинергические препараты, агонисты дофаминовых рецепторов, L-допа-содержащие препараты, амантадины. Антихолинергические препараты (тригексифенидил, бипериден) обладают центральным и периферическим холинолитическим эффектом, могут назначаться в дозировке 1-2 мг 3 раза в сутки. Применяются, прежде всего, у пациентов молодого и среднего возраста. В настоящее время циклодол редко используют в связи с его частыми побочными эффектами (сухость во рту, запоры, задержка мочеиспускания, психотические нарушения). Агонисты дофаминовых рецепторов (мирапекс, проноран, апоморфин) воздействуют на тремор путем прямой стимуляции специфических Д1, Д2, Д3 рецепторов, обеспечивают равномерный синтез и высвобождение дофамина, не индуцируют антиоксидантный стресс. Лечение начинают с малых доз с постепенным наращиванием дозы до 150 мг/сут. В последние годы начал применяться метод введения апоморфина с помощью особой помпы, эффективность которого сопоставима с нейрохирургическим вмешательством. L-допа-содержащие препараты (наком, мадопар, синдопа, синемет) представляют собой метаболические предшественники дофамина. Эффективность их воздействия на дрожание существенно меньше, чем на ригидность и акинезию. Средняя терапевтическая доза составляет 500-750 мг/сут. Увеличение дозы приводит к моторным флюктуациям и дискинезиям. Амантадины (ПК-Мерц, мидантан) с успехом применяются для лечения акинезии и ригидности у пациентов с болезнью Паркинсона и симптоматическим паркинсонизмом. Нам не встретилось работ о влиянии амантадинов на паркинсонический тремор. Поэтому в июне - ноябре 2006 г. на базе 2-го неврологического отделения 5-й городской клинической больницы г. Минска нами проведено клиническое исследование по оценке эффективности инфузионной формы ПК-Мерца на дрожание в комплексном лечении болезни Паркинсона.
Обследовано 30 больных (17 мужчин, 13 женщин, средний возраст 67,2 ± 14,7 года) со II, III стадиями болезни Паркинсона. Диагноз был установлен на основании общепринятых диагностических критериев. Степень тяжести по Хену и Яру составила 2,5 ± 0,5. Длительность заболевания была 6,4 ± 2,5 года. Дрожательноригидная форма заболевания выявлена у 12 человек, ригиднодрожательная форма - у 18 человек. 27 больных исследуемой группы ранее получали ДОФА-препараты (мадопар, наком) в дозе 500-750 мг/сут. Критерием исключения из исследования было наличие у больных общеизвестных противопоказаний к назначению ПК-Мерц. Дизайн исследования включал неврологический осмотр с клинической оценкой выраженности тремора, ригидности, акинезии и постуральной неустойчивости. Для исключения иной этиологии синдрома паркинсонизма всем пациентам выполнена КТ или МРТ головного мозга. Объективизация тремора проведена при помощи акселерометров типа ADXL103. В исследовании применен внешний аналогово-цифровой преобразователь ADCS5K-12-8, подключенный к COM-порту компьютера, для преобразования электрических сигналов, получаемых при движении датчиков, в цифровые и их ввода в компьютер. Для обработки данных использовали программу OriginPro 7-й версии. Датчики прикрепляли к проксимальной фаланге большого пальца кисти. При регистрации тремора покоя пациент сидел на стуле, руки свободно лежали на коленях. Постуральный тремор фиксировали при вытянутых вперед руках, кинетический - при пальценосовой пробе. Каждый вид тремора регистрировали в течение 32 сек. ПК-Мерц назначали в дозе 500 мл (200 мг) внутривенно капельно ежедневно 2-4 инфузии на курс с последующим приемом препарата внутрь в дозе 200-400 мг/сут. Обследование производили до и после инфузии препарата. Полученные результаты обработаны с помощью программы «Статистика» с предварительной оценкой параметров распределения выборки. Сравнение состояния тремора у больных до и после лечения основывалось на определении критерия Вилкоксона.
До лечения у всех больных обследуемой группы отмечали в конечностях мелко- и среднеамплитудный ритмичный тремор покоя и постуральный, умеренную гипокинезию и повышение мышечного тонуса типа «зубчатого колеса», которые носили асимметричный характер. У 30% больных имела место постуральная неустойчивость, которая проявлялась в падениях и в нарушении равновесия при резких поворотах, была положительной проба Тавенарда. У 1 пациентки имела место лекарственная дискинезия в форме мышечной дистонии (дистония пика дозы) на фоне приема ДОФА-препаратов. При проведении КТ (МРТ) головного мозга во всех случаях обнаруживали расширение субарахноидальных пространств на конвексе, базальных цистерн и желудочковой системы без признаков очагового поражения мозга. При акселерометрии до лечения были получены следующие характеристики паркинсонического тремора: покоя - частота 4,5 Гц, амплитуда 48-2388 ед.; постуральный - частота 5,5 Гц, амплитуда 71-3187 ед.; спектра кинетического дрожания зафиксировано не было.
На фоне проводимой терапии наряду с регрессом экстрапирамидной ригидности и гипокинезии у 3 пациентов (10%) достигнуто полное исчезновение постурального тремора и тремора покоя. Еще у 6 пациентов (20%) было отмечено исчезновение постурального дрожания и уменьшение тремора покоя. В 16 случаях (53,3%) - одновременное значительное уменьшение тремора покоя и постурального тремора (амплитуда дрожания уменьшилась более чем на 50% согласно данным акселерометрии). Влияния препарата на частоту паркинсонического дрожания во время лечения зафиксировано не было.
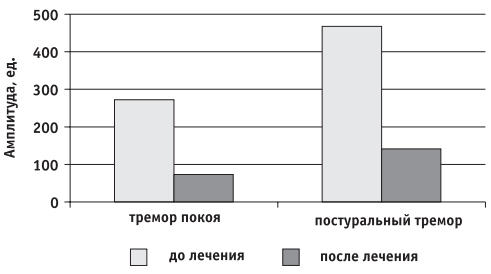
Рис. Динамика амплитуды тремора до и после лечения инфузионной формой препарата ПК-Мерц.
Результаты влияния препарата на амплитуду дрожания приведены на рисунке: до лечения амплитуда тремора покоя в исследуемой группе составила: медиана - 272 ед.; 25-й перцентиль - 112 ед.; 75-й перцентиль - 611 ед.; среднее отклонение - 641. После лечения амплитуда тремора достоверно уменьшилась: медиана - 73 ед.; 25-й перцентиль - 29 ед.; 75-й перцентиль - 149 ед.; среднее отклонение - 134 (p
Отсутствие эффекта от всех видов консервативного лечения во всем мире является показанием для нейрохирургического вмешательства. Паллидарная стимуляция и стимуляция субталямического ядра являются в настоящее время наиболее современными хирургическим вмешательствами для уменьшения тремора.
Таким образом, тремор является наиболее частым проявлением гиперкинетического синдрома, обладает существенным клиническим полиморфизмом, затрудняющим его диагностику. Существенную пользу в распознавании тремора приносят инструментальные методы. Одним из современных методов регистрации дрожания является акселерометрия. Подход медика к лечению тремора должен быть дифференцированным, индивидуальным и ступенчатым. В терапии паркинсонического дрожания показано применение инфузионной формы препарата ПК-Мерц. При отсутствии эффекта прибегают к политерапии или нейрохирургическому вмешательству.
Пономарев В. В., Бойко А. В. 5-я ГКБ г. Минска.
Опубликовано: журнал «Медицинская панорама» № 5, апрель 2007 года.