Начало: бета-адреноблокаторы в лечении хронической сердечной недостаточности.
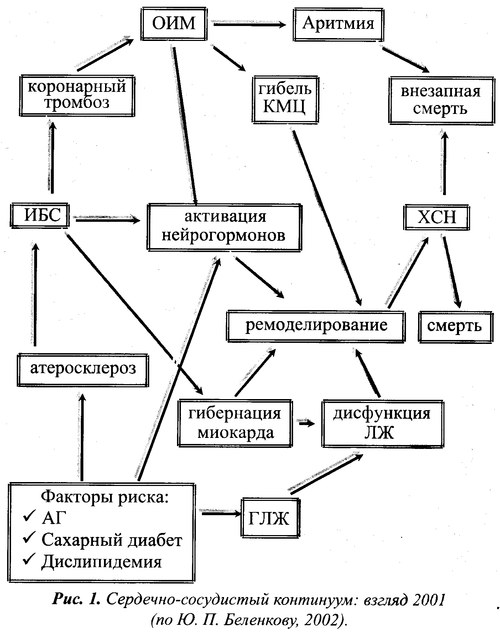
По определению Ю. Н. Беленкова (2002) процесс непрерывного развития сердечно-сосудистых заболеваний - от факторов риска до гибели пациента есть единый сердечно-сосудистый континуум (рис. 1.). Как видно из представленного рис., этот процесс от появления главных факторов риска (ФР) — артериальной гипертензии (АГ), сахарного диабета (СД) и дислипидемии, способных привести к ишемической болезни сердца (ИБС), которая может осложниться развитием острого инфаркта миокарда (ОИМ), до ремоделирования левого желудочка (ЛЖ) вследствие гибели кардиомиоцитов (КМЦ) и потери сократительной способности миокарда может протекать достаточно продолжительно. Интенсивность развития ХСН, приводящей к смерти пациента, во многом определяется как количеством погибших кардиомиоцитов, так и качеством лечения пациента. В то же время гибель больного, особенно у лиц с начальными проявлениями ХСН, может быть вследствие появления жизненно опасных аритмий. Развитие ХСН может идти и иным путем: артериальная гипертензия → гипертрофия левого желудочка → дисфункция левого желудочка → ХСН или ИБС → гибернация миокарда → дисфункция левого желудочка → ХСН.
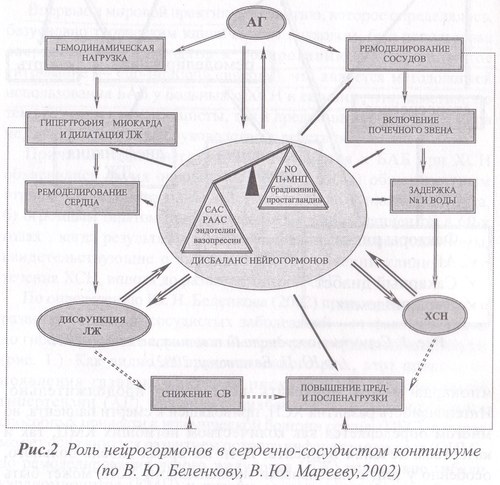
Необходимой стадией развития сердечно-сосудистого континуума является ремоделирование сердечной мышцы. По определению М. Pfeffer (1985) "ремоделирование — это структурно-геометрические изменения левого желудочка, включающие в себя процессы гипертрофии миокарда и дилатации сердца, приводящие к изменению его геометрии и нарушению систолической и диастолической функции". Как видно из вышеприведенного рис., одним из важнейших путей прерывания порочного круга ремоделирования сердечной мыщцы является воздействие на его главное звено патогенеза — гиперактивацию нейрогормональных систем, роль которых в сердечно-сосудистом континууме может быть схематично представлена следующим образом (рис.2).
В результате перегрузки сердца давлением, как, например, при артериальной гипертензии, развивается концентрический тип гипертрофии стенок левого желудочка (рис.3). За счет утолщения стенок левого желудочка (увеличения его полости при этом нет) повышается жесткость миокарда, т.е. развивается так называемая диастолическая дисфункция левого желудочка (ДДЛЖ). При таком изменении структуры левого желудочка меняется и его функция, в данном случае наблюдается недостаточное диастолическое расслабление левого желудочка. Второй тип ремоделирования развивается по иному механизму, когда результатом структурной перестройки сердечной мышцы является эксцентрическая гипертрофия левого желудочка.
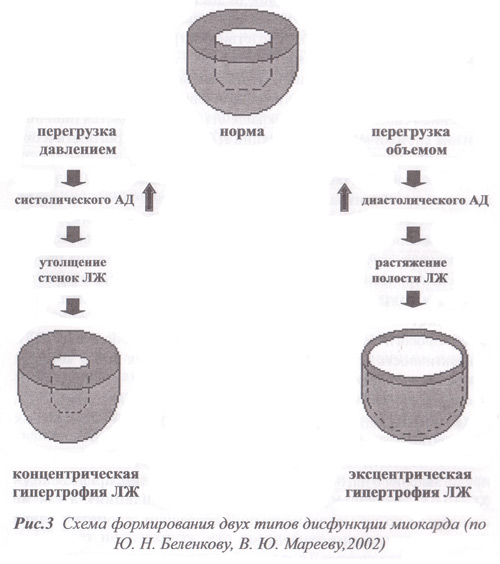
Суть процесса перестройки геометрии левого желудочка заключается в следующем. При объемной перегрузке, возникающей, например, при гемодинамически значимой недостаточности митрального клапана, ситуации нередкой у пациентов ранее перенесших острый инфаркт миокарда (ОИМ), вследствие митральной регургитации развивается эксцентрическая гипертрофия левого желудочка и расширение его полости. Подобная ситуация, усугубляющаяся ишемией миокарда, ведущей к гибели кардиомиоцитов, сопровождается существенным снижением силы сердечного сокращения, т.е. наблюдается типичная картина систолической дисфункции левого желудочка (СДЛЖ), прогностически более неблагоприятной, чем диастолическая дисфункция левого желудочка.
Резюмируя представленные данные, не останавливаясь на других важнейших механизмах формирования недостаточности миокарда, выделим главное. На длинном пути от дисбаланса нейрогормонов, определяющих степень и интенсивность клеточного повреждения до появления структурного изменения самой мышцы сердца, вплоть до эксцентрического ремоделирования, у большинства пациентов проходят годы. Этапность сердечно-сосудистого континуума позволяет полезно воздействовать на ключевые звенья патофизиологического процесса развития и прогрессирования ХСН. Эффективность применения нейромодуляторов, к числу которых относятся, в первую очередь, ингибиторы ангиотензинпревращающего фермента (иАПФ) и бета-адреноблокаторы, доказана огромным числом масштабных многоцентровых кооперативных исследований.
Тем не менее, даже несмотря на достаточно четкие представления о патофизиологии основных причин, приводящих к ХСН (артериальной гипертензии, сахарного диабета (СД) и дислипидемии), а так же стандартов по их медикаментозной коррекции, прогноз течения ХСН остается пессимистическим.
В качестве одной из причин развития ХСН можно отметить ситуацию у больных с артериальной гипертензией — основной категории пациентов, у которых формируется дисфункция миокарда. В России по данным И. Е. Глазовой (2002), базирующихся на исследованиях сотрудников центра профилактической медицины РФ, артериальной гипертензией страдают 41,1% женщин старше 18 лет и 39,2% мужчин. Тем не менее, несмотря на такую высокую распространенность артериальной гипертензии (по данным обследования 80000 человек в возрасте 40-45 лет в 23-х городах России в среднем артериальная гипертензия в популяции составила 23%), о наличии заболевания знали лишь 57% больных, а эффективным лечение было признано только в 8% случаев. Эффективно лечатся только 27% пациентов с артериальной гипертензией в США, Италии - 9%, Египте - 8%, Англии - 6%, Китае - 3%, Польше - 2 %.
Исходя из этого немаловажного и только одного примера, перед врачом-практиком возникает вопрос: что же делать, чтобы лиц с дисфункцией миокарда было как можно меньше и какими способами это можно осуществить? Что делать, если применение таких испытанных временем и опытом клиницистов популярных антигипертензивных средств, как резерпин, адельфан и др., например, еще более популярного клонидина (клофелина), является свидетельством некомпетентности терапевта в области современной кардиологии и в конечном итоге ведет к увеличению случаев смертей от инсульта у больных с артериальной гипертензией, особенно в сочетании ее с ХСН?